 |
Cash+Carry Angehrn:
Frische für Profis
an neun Standorten
in der Deutschschweiz.
Direkt zur
CCA-Website:
www.cca-angehrn.ch
|


Schweizerischer Bäckerei- und Konditorei-Personal-Verband
|
|
 |
 |
 |
 |
| 20.1.2012 - Rubrik: Fleisch & Delikatessen
| Druckansicht | Wie riskant ist Transglutaminase in Fleischwaren?
Das Enzym Transglutaminase (TG) wird oft als Kleber verwendet, um einzelne kleinere Fleischteile zu grossen Fleischstücken zusammenzusetzen. Eingesetzt wird dabei üblicherweise Transglutaminase mikrobiellen Ursprungs (mTG). In der Öffentlichkeit wurde das Enzym in der Vergangenheit im Zusammenhang mit so genanntem Klebeschinken diskutiert. Das BfR informiert, dass ein klinisches Risiko für Zöliakie-Patienten durch mTG nicht auszuschliessen ist, da Studien dazu noch fehlen. Nach einer Erhitzung sei ein allfälliges Risiko jedoch nicht mehr vorhanden.
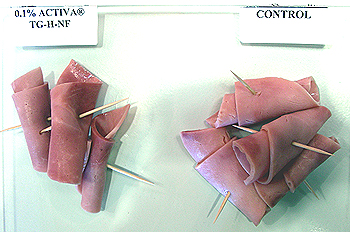
Muster aus Versuchen des japanischen Enzymherstellers Ajinomoto mit dem Kleb-Enzym Transglutaminase, das sehr effizient Proteinmoleküle vernetzt - eine umstrittene Methode zum Restrukturieren von grossen aus kleinen Fleischstücken (Formfleisch).
|
Birgt Transglutaminase mikrobiellen Ursprungs (mTG), wenn sie einem Lebensmittel zugesetzt wird, gesundheitliche Risiken für Zöliakie-Patienten? Erkenntnisse zu mTG in "Enzymklebeschinken" lassen gemäss dem deutsche Bundesinstitut für Risikobewertung (BfR) nicht darauf schliessen, dass vom Enzym selbst (auch in aktiver Form) bei gesunden Personen ohne Beeinträchtigung der Verdauungsfunktion ein relevantes gesundheitliches Risiko ausgeht.
Bekannt ist, dass mTG verschiedene Proteinverbindungen bilden kann ("enzymatic cross-linking"). Deren Bewertung ist derzeit mangels ausreichender Daten nicht möglich. Dem BfR liegen Hinweise aus experimentellen Untersuchungen vor, dass mTG zusammen mit Nahrungsproteinen zu Verbindungen führen kann, die strukturell vergleichbar mit Gluten sind, das bei Zöliakie-Patienten die bekannten immunologischen Effekte bewirkt.
Ob sich daraus jedoch für diese Patienten gesundheitliche Risiken wie die typische Schädigung der Darmschleimhaut ergeben, ist gegenwärtig nicht sicher geklärt. Ausreichende klinische Studien liegen hierzu nicht vor, insofern ist ein klinisch relevantes Risiko für Zöliakie-Patienten durch mikrobielle Transglutaminase möglich.
Eine geeignete Kennzeichnung von Lebensmitteln, die unter Verwendung von mTG hergestellt werden, würde es diesen Patienten ermöglichen, den in der Wissenschaft noch weiter zu klärenden Unsicherheiten aus dem Wege zu gehen.
Darüber hinaus wären bei entsprechender Lebensmittelkennzeichnung auch alle Verbraucher über den Einsatz des Enzym-Klebers besser informiert. Im Lebensmittelprodukt kann mTG etwa durch thermische Behandlung inaktiviert werden. Die Daten deuten darauf hin, dass ein Risiko für Zöliakie-Betroffene, sollte es überhaupt bestehen, dadurch praktisch auszuschliessen wäre. Entscheidend ist nach wie vor, dass Zöliakie nur dann beherrschbar ist, solange Patienten vollständig auf Gluten verzichten.
1 Gegenstand der Bewertung
In der Diskussion um das Enzym Transglutaminase, welches bei der Lebensmittelverarbei-tung u. a. zur Herstellung von sogenanntem "Klebeschinken" verwendet wird, wird auch auf mögliche gesundheitliche Risiken hingewiesen, insbesondere für Patienten mit Zöliakie. In diesem Zusammenhang hat das BfR die Frage möglicher gesundheitlicher Risiken bei der Verwendung von Transglutaminase geprüft und nimmt aus Sicht der Risikobewertung Stellung.
Dem Bundesinstitut für Risikobewertung (BfR) liegt eine Stellungnahme eines Herstellers von Transglutaminase zu dieser Fragestellung vor, wonach es keine Erkenntnisse dazu gebe, dass die Verwendung von Transglutaminase bei der Lebensmittelverarbeitung für Zöliakie-Patienten ein besonderes gesundheitliches Risiko darstelle (Firma Ajinomoto Europe S.A.S., 75817 Paris, 19.04.2010). Die genannte Firma stellt kommerziell mikrobielle Transglutaminase (mTG aus dem Bakterium Streptoverticillium mobaraense) zur Verwendung bei der Lebensmittelverarbeitung her.
Des weiteren liegt dem BfR ein Bericht der "IG Zöliakie der Deutschen Schweiz" vom 07.05.2010 vor, wonach in der schweizerischen Verbraucherzeitschrift "k-tipp", Ausgabe
9/2010, darauf hingewiesen wird, dass das schweizerische Bundesamt für Gesundheit (BAG) beabsichtigt, einen Verbraucherhinweis für mit Transglutaminase hergestellte Fleischerzeugnisse einzuführen, insbesondere um Zöliakie-Betroffene zu informieren (http://www.zoeliakie.ch/news/artikel /transglutaminase-schaedlich-fuer-zoeliakie-betroffene/).
Der in der Schweiz inzwischen vorgeschriebene Verbraucherhinweis betrifft Produkte, die unmittelbar zum Verzehr bestimmt sind. Produkte, die vor dem Verzehr erhitzt werden, sind von dem Hinweis nicht betroffen (http://www.zoeliakie.ch/news/artikel/mit-transglutaminasebehandeltes-fleisch/).
2 Ergebnis
Die im BfR vorliegenden Erkenntnisse zu mikrobieller Transglutaminase (mTG) bei der Verwendung zur Rekonstitution bzw. Restrukturierung von Fleischabschnitten ("Enzymklebeschinken") geben nicht zu der Vermutung Anlass, dass von dem Enzym selbst (auch in aktiver Form) in Lebensmitteln bei gesunden Personen ohne Beeinträchtigung der physiologi-schen Magen- und Verdauungsfunktion ein relevantes gesundheitliches Risiko ausgeht. Allerdings sind belastbare Aussagen über Konsequenzen, die sich aus der Aufnahme der durch Verwendung von mikrobieller Transglutaminase gebildeten verschiedenen Proteinverbindungen ("enzymatic cross-linking") für den Menschen ergeben können, derzeit mangels ausreichender Daten nicht möglich.
Hinsichtlich der Zöliakie ist festzustellen, dass Hinweise aus experimentellen Untersuchun-gen - darunter auch Bestimmungen immunologischer Parameter beim Menschen - vorliegen, dass mikrobielle Transglutaminase zusammen mit Nahrungsproteinen, insbesondere aus Getreide, zu bestimmten Epitopen (antigene Determinanten) führen kann. Diese Epitope sind strukturell vergleichbar mit denen des Glutens, welche bei Zöliakie die bekannten immunologischen Effekte bewirken. Inwieweit man aus diesen Hinweisen relevante Effekte auf die klinische Situation von Menschen mit Zöliakie ableiten kann und sich daraus für diese Patienten gesundheitliche Risiken wie die typische mukosaschädigende Wirkung ergeben, ist zum gegenwärtigen Zeitpunkt nicht sicher geklärt. Ausreichende klinische Studien liegen hierzu nicht vor.
Ein klinisch relevantes Risiko ist mit geringer Wahrscheinlichkeit möglich. Der Vorschlag aus der Schweiz, Lebensmittel mit mikrobieller Transglutaminase speziell für Zöliakie-Betroffene zu kennzeichnen, könnte hilfreich sein, da diesen Patienten damit ermöglicht würde, den bestehenden und in der Wissenschaft noch weiter zu klärenden Unsicherheiten aus dem Wege zu gehen. Die Daten deuten darauf hin, dass ein möglicherweise bestehendes Risiko für Zöliakie-Betroffene minimiert bzw. praktisch auszuschliessen wäre, wenn mTG im Lebensmittelendprodukt inaktiviert wird, etwa durch ausreichende thermische Behandlung. Entscheidend ist nach wie vor, dass Zöliakie nur dann beherrschbar ist, solange die übliche Gluten vermeidende Diät eingehalten wird.
Das BfR macht darauf aufmerksam, dass eine Rekonstitution von Fleischabschnitten mittels mikrobieller Transglutaminase - zumindest wenn das verwendete Enzym und die spezifische Produktverarbeitung nicht gekennzeichnet werden - zu einer Irreführung der Verbraucherinnen und Verbraucher führen kann.
Die vorliegende Stellungnahme lässt möglicherweise bestehende hygienische Bedenken gegenüber der Rekonstitution von Fleischabschnitten mittels mikrobieller Transglutaminase unberücksichtigt. Auch ist die vorliegende gesundheitliche Bewertung keine Sicherheitsbewertung von Quelle und Herstellungsprozess der in Rede stehenden mikrobiellen Transglutaminase (mTG aus Streptoverticillium mobaraense) zur Verwendung in der Lebensmitteltechnologie. Das BfR verweist auf die Verordnung (EG) Nr. 1332/2008 vom 16.12.2008, welche den Einsatz von Lebensmittelenzymen, die aus technologischen Gründen in Lebensmitteln eingesetzt werden, weitergehend regelt, u. a. durch Erstellung einer Positivliste.
3 Begründung
Transglutaminasen (TG) gehören zu einer Gruppe von Enzymen, die in der Natur weit verbreitet sind, z. B. in Mikroorganismen, im Muskelfleisch von Fischen, in Muscheln, aber auch in der Leber und im Blut von Säugetieren sowie beim Menschen. Beim Menschen sind mehrere Isoenzyme bekannt. Es handelt sich um Enzyme aus der Klasse der Transferasen. Transglutaminasen katalysieren Acyl-Transfer-Reaktionen (zwischen γ-CarboxyamidGruppen von proteingebundenem Glutamin), Desamidierungen und die (Quer-)Vernetzung von Proteinen (Isopeptidbindungen, v. a. zwischen Lysin und Glutamin). Im menschlichen Organismus sind verschiedene Transglutaminasen mit Funktionen z. B. bei der Blutgerinnung sowie beim Gewebeaufbau beschrieben (Malandain, 2005). Vereinfacht gesagt sind Transglutaminasen "biologische Kleber", die hochmolekulare Proteinstrukturen aufbauen.
In der Lebensmittelverarbeitung wird Transglutaminase (IUBMB Enzyme Nomenclature: EC 2.3.2.13, CAS-Nr. 80146-85-6, chemischer Name: Protein-Glutamin -Glutamyltransferase, http://www.chem.qmul.ac.uk /iubmb/enzyme/EC2/3/2/13.html) als Verarbeitungshilfsstoff z. B. für die Herstellung von rekonstituiertem Fleisch oder Fisch eingesetzt. Das Enzym hat bei der Herstellung von Lebensmitteln einen erheblichen Einfluss auf Eigenschaften wie Textur, Festigkeit und Elastizität, zum Teil auch auf den Geschmack der Endprodukte. Es kann verwendet werden, um Fleischabschnitte wieder zu grösseren Stücken zusammenzufügen ("Klebeschinken", genauer gesagt "Enzymklebeschinken") sowie bei der Verarbeitung von Brühwurstwaren und der Herstellung von Surimi aus Fischabschnitten.
Auch Proteine in Lebensmitteln pflanzlicher Herkunft können mit Transglutaminase behandelt werden (Dube et al., 2007; De Jong/Koppelman, 2002; Kantonales Laboratorium Thurgau, Jahresbericht 2002, http://www.kantlab.tg.ch/documents/Jahresbericht_2002.pdf; Aalami/Leelavathi, 2008). Untersuchungen zeigen, dass eine thermische Behandlung von zwei Minuten Dauer bei einer Temperatur von 80°C eine Inaktivierung des Enzyms bewirkt (Menendez et al., 2006). Hinweise auf eine mögliche Beeinflussung der Allergenität von Proteinen durch Transglutaminase liegen vor, möglicherweise im Sinne einer Abnahme (Zhu/Tramper, 2008; Malandain, 2005).
Ein besonderes allergenes Potential des Enzyms selbst ist aufgrund vorliegender Daten nicht anzunehmen (Dube et al., 2007; Pedersen, 2004). Neben Transglutaminase wird mit ähnlicher Zweckbestimmung auch der Stoff Thrombin in der Lebensmittelverarbeitung eingesetzt (Österreichische Agentur für Gesundheit und Ernährungssicherheit, AGES, http://www.ages.at/ages/ernaehrungssicherheit/ thema-ernaehrung/faq-klebefleisch/). Das BfR macht in diesem Zusammenhang auf die kritische Diskussion des EU-Parlaments zum Einsatz von Thrombin für die Verwendung in Lebensmitteln zur Rekonstitution von Fleischabschnitten im Mai 2010 aufmerksam.
Nach Kenntnis des BfR ist die in der Lebensmittelindustrie kommerziell genutzte Transglutaminase mikrobiellen Ursprungs (mikrobielle Transglutaminase, mTG aus dem Bakterium Streptoverticillium mobaraense) chemisch eine Polypeptidkette mit einem Molekulargewicht von 38000 Da und besteht aus 331 Aminosäuren mit einem Cystein-Rest im aktiven Zentrum (http://www.ajinomoto.de/cms/ front_content.php?idcat=99; Kikuchi et al., 2003; Engel et al., 2000; Zellner , 2000).
Dem BfR ist das Ausmass der Verwendung von mikrobieller Transglutaminase bei der Lebensmittelverarbeitung nicht bekannt, ebenso wenig, welche Mengen des Enzyms bei welchen Lebensmitteln eingesetzt werden und welche Enzym-Mengen im jeweiligen Endprodukt
auch in aktiver Form - vorliegen und vom Verbraucher verzehrt werden. Gemäss Angaben des Herstellers Ajinomoto Europe liegt im Enderzeugnis keine technologische Wirkung von mTG mehr vor, selbst wenn inaktive Reste technisch unvermeidbar wären (http://www.transglutaminase.com /de/news-1, Krell, Weyland, Grube, 2010).
Unter Vorbehalt werden Literaturangaben zitiert, wonach mit einer maximalen täglichen Aufnahme von mTG über Lebensmittel von geschätzt etwa 8-13 mg, bis zu 15 mg zu rechnen wäre und zur Rekonstitution bei der Lebensmittelverarbeitung pro Kilogramm Lebensmittel ca. 50-100 mg mTG eingesetzt werden (Malandain, 2005; Pedersen, 2004).
Über Versuche aus der Le-bensmitteltechnologie, mit Mengen bis zwei Gramm mTG pro Kilogramm Lebensmittel bei der Brühwurstherstellung zu arbeiten, wurde berichtet (Eberhard et al., 2009). Mikrobielle Transglutaminase hat in den USA von der Food and Drug Administration (FDA) den GRAS-Status (Generally Recognized As Safe) erhalten. Dabei werden Enzymmengen in verschie-denen Lebensmitteln von 25 ppm (parts per million) bis 250 ppm angegeben (http://www.accessdata.fda.gov/ scripts/fcn/gras_notices/grn0095.pdf).
In der Schweiz wird Transglutaminase nicht als Verarbeitungshilfsstoff beurteilt, sondern als kennzeichnungspflichtige Zutat.
Dort unterstehen rekonstituierte Lebensmittel, die unter Einsatz von mikrobieller Transglutaminase (mTG) hergestellt werden, gemäss Artikel 5 Absatz 1 der Lebensmittel- und Gebrauchsgegenständeverordnung (SR 817.02) der Bewilligungspflicht. Darüber hinaus müssen Erzeugnisse, die mit Transglutaminase hergestellt wurden, entsprechend gekennzeichnet werden, da sie für den durchschnittlich informierten Verbraucher in ihrer Form und ihrer sonstigen Erscheinung kaum von natürlich gewachsenen Fleischstücken zu unterscheiden sind. Deshalb soll in der Schweiz in der Produktkennzeichnung sowohl auf die Rekonstitution, als auch auf die Natur der verwendeten Klebestoffe (hier: Transglutaminase) hingewiesen werden.
Bei der Pathogenese der Zöliakie (Enteropathie infolge immunologisch bedingter Unverträglichkeit von Gluten/Gliadin aus Weizen und bestimmten anderen Getreiden) spielt körpereigene Gewebs-Transglutaminase (tissue-Transglutaminase, tTG) eine wichtige Rolle, u. a. bei der Präsentation der Antigene gegenüber bestimmten Immunzellen. Die Zöliakie geht mit einer erhöhten Aktivität der Gewebs-Transglutaminase (tTG) in den Darmepithelzellen einher. Die Bestimmung von IgA-Antikörpern gegen tTG ist ein wichtiger diagnostischer Parameter.
Die Funktion der tTG wird in der wissenschaftlichen Diskussion in Verbindung gestellt mit der Überlegung, dass mTG zusammen mit Nahrungsproteinen, insbesondere aus Getreide, bestimmte Epitope (antigene Determinanten) bilden können, die strukturell vergleichbar sind mit denen des durch tTG veränderten Glutens, welche bei Zöliakie-Betroffenen die typischen Entzündungsprozesse bewirken (Gerrard/Sutton, 2005; Dube et al., 2007; Cabrera-Chavez et al., 2008 und 2009; Malandain, 2005). Es kann nicht ausgeschlossen werden, dass aktive mTG in Lebensmitteln die intestinale Immunoreaktivität steigern und eine Verstärkung des Entzündungsprozesses triggern, auch wenn hierfür bisher lediglich in vitro- und ex vivo-Daten vorliegen (Berti et al., 2007, Cabrera-Chavez et al., 2008, 2009).
Daneben werden in der wissenschaftlichen Diskussion auch Aspekte angesprochen, inwieweit eine "Detoxifizierung" von Gluten mittels kontrollierter Behandlung mit Transglutaminase möglich sein könnte, mit dem Ziel, diese Proteine künftig für Zöliakie-Betroffene verträglich machen zu können. Hierzu liegen experimentelle Untersuchungen vor (Schuppan/Junker, 2007; Gianfrani et al., 2007; Berti et al., 2007), die Daten und vorläufigen Erkenntnisse zu diesem Aspekt sind jedoch im Wesentlichen unzureichend.
Aktualisierte Stellungnahme Nr. 052/2011 des BfR vom 30. November 2011
Wissenswertes über Lebensmittelenzyme
Enzyme sind Eiweisse, die wichtige Funktionen im Stoffwechsel von Organismen ausüben. Als Biokatalysatoren beschleunigen sie biochemische Reaktionen, die z.B. bei der Verdauung von Lebensmitteln im Magen-Darmtrakt und in den Zellen der Gewebe ablaufen.
Lebensmittelenzyme werden Lebensmitteln zugesetzt, um z.B. bei der Herstellung, Verarbeitung, Zubereitung, Behandlung oder Lagerung von Lebensmitteln einen technologischen Zweck zu erfüllen. Sie werden aus Pflanzen, Tieren oder Mikroorganismen gewonnen, häufig auch durch ein Fermentationsverfahren mit Mikroorganismen. Einige Lebensmittelenzyme werden unter Verwendung gentechnisch veränderter Mikroorganismen hergestellt.
Gesetzliche Regelungen
Nur wenige Lebensmittelenzyme waren in der Europäischen Union (EU) bis zum Inkrafttreten der Verordnungen (EG) Nr. 1331/2008 über das einheitliche Zulassungsverfahren für Lebensmittelzusatzstoffe, Enzyme und Aromastoffe und Nr. 1332/2008 über Lebensmittelenzyme einheitlich geregelt. Dabei handelte es sich um Invertase (E 1103) und Lysozym (E 1105), die als Lebensmittelzusatzstoffe klassifiziert wurden.
Darüber hinaus bestanden produktspezifische Regelungen für bestimmte Enzyme zur Verwendung in Wein (Urease, beta-Glucanase und Lysozym), für Lab und andere milchkoagulierende Enzyme bei der Käseproduktion sowie für einige Enzyme bei der Fruchtsaftherstellung. Die Mehrzahl der verwendeten Enzyme, die als Verarbeitungshilfsstoffe angesehen wurden, unterlag dagegen einzelstaatlichen Regelungen, in Deutschland den Bestimmungen des Lebensmittel-, Bedarfsgegenstände- und Futtermittelgesetzbuchs (LFGB).
Durch die beiden neuen Verordnungen ist nun das Inverkehrbringen, die Verwendung und Kennzeichnung aller Lebensmittelenzyme, auch die als Verarbeitungshilfsstoffe verwendeten Enzyme, EU-weit einheitlich geregelt. Die zur Verwendung zugelassen Enzyme sollen in eine Gemeinschaftsliste aufgenommen werden, wenn sie folgende Bedingungen erfüllen:
ihre Verwendung bei der vorgeschlagenen Dosis ist für den Verbraucher gesundheitlich unbedenklich, soweit die verfügbaren wissenschaftlichen Daten ein Urteil hierüber erlauben,
es besteht eine hinreichende technologische Notwendigkeit für die Verwendung und
der Verbraucher wird durch die Verwendung nicht irregeführt.
Die erstmalige Erstellung der Liste wird in einem Schritt erfolgen, nachdem die dafür erforderlichen gesundheitlichen Bewertungen abgeschlossen sind. Bis zur Annahme der Gemeinschaftsliste bleiben die einzelstaatlichen Regelungen in Kraft. (Text: BFR)
| | __________________________________________ |
 | |
 |
 |
|
 |