Varia | ||||
| 22.5.2012 ZHAW-Lebensmittelrechts-Tagung: Rückblick
Die diesjährige Wädenswiler Lebensmittelrechts-Tagung vom 10. Mai 2012 thematisierte die jüngsten wichtigen Entwicklungen im EU-Lebensmittelrecht. Diese sind auch aus Sicht der Schweiz von Bedeutung, weil viele Schweizer Firmen in den EU-Raum exportieren und sich die Schweiz zudem bei der Revision und Weiterentwicklung ihres nationalen Rechts an der EU orientiert. Das neue EUKennzeichnungsrecht wurde an der Tagung behandelt, ebenso wie die Entwicklungen im Zusatzstoffrecht sowie bezüglich den Health Claims (gesundheitsbezogenen Angaben). Zudem wurde dargelegt, welchen Einfluss diese Entwicklungen in der EU auf das Schweizer Lebensmittelrecht nehmen. Rund 180 Personen haben die Tagung besucht. In der Einführung zur Tagung wies Evelyn Kirchsteiger-Meier, Dozentin und Tagungsleiterin, darauf hin, dass 2012 ein besonderes Jubiläumsjahr für das europäische Lebensmittelrecht darstellt: Die sogenannte EU-Basisverordnung Nr. 178/20021, mit der das EU-Lebensmittelrecht und die Lebensmittelsicherheit auf eine neue Grundlage gestellt wurden, feiert ihr 10jähriges Jubiläum. Trotzdem war dieser runde Geburtstag nicht der Auslöser für die Wahl des Tagungsthemas Update EU-Lebensmittelrecht, denn es bestehen genügend andere wichtige Themen, in denen der EU-Gesetzgeber in den vergangenen Monaten aktiv war und die an der Tagung behandelt wurden. Neuordnung des EU-Kennzeichnungsrechts Die ersten beiden Referate des Tages legten die wichtigsten Punkte der neuen Lebensmittelinformationsverordnung Nr. 1169/2011 (LMIV)2 dar. Nach langen, kontroversen und schwierigen Diskussionen wurde sie am 22. November 2011 im EU-Amtsblatt veröffentlicht. Sie löst verschiedene Richtlinien ab, so die bisherige Etikettierungsrichtlinie 2000/13/EG. Es gilt, die Pflichtangaben gemäss Art. 9 und 10 LMIV einzuhalten. Nachfolgend die wichtigen neuen Punkte des EU-Kennzeichnungsrechts, die an der Tagung erläutert wurden. Obligatorische Nährwertdeklaration Angabe des Brennwerts, von Fett, gesättigten Fettsäuren, Kohlenhydraten, Zucker, Eiweiss und Salz (Big 7) bezogen auf 100 g oder 100 ml in einer übersichtlichen Tabelle, wie sie im Anhang XV der Verordnung aufgeführt ist. Die vorgegebene Reihenfolge ist einzuhalten. Zudem ist es möglich, auf freiwilliger Basis noch folgende Stoffe in der Nähwertdeklaration aufzuführen: einfach ungesättigte Fettsäuren, mehrfach ungesättigte Fettsäuren, mehrwertige Alkohole, Stärke, Ballaststoffe, bestimmte Vitamine und Mineralstoffe in signifikanten Mengen (siehe Art. 30 LMIV). Es handelt sich hierbei um eine abschliessende Liste; die Auflistung weiterer Stoffe wie Cholesterin oder Transfettsäuren ist nicht erlaubt. Zu letzteren ist die Kommission beauftragt, innerhalb von 3 Jahren einen Bericht vorzulegen, der u.a. aufzeigen soll, ob die Bereitstellung von Verbraucherinformationen über Transfettsäuren die Förderung an gesünderen Lebensmitteln für die Verbraucher zur Folge hat. Auf der Vorderseite (Hauptsichtfeld) der Verpackung kann auf freiwilliger Basis die Information über bestimmte Nährstoffe wiederholt werden: der Brennwert oder der Brennwert zusammen mit den Mengen an Fett, gesättigten Fettsäuren, Zucker und Salz (Big 5, anzugeben pro 100 g/100 ml oder pro Portion, dann muss der Brennwert zusätzlich pro 100g / 100 ml angegeben werden). 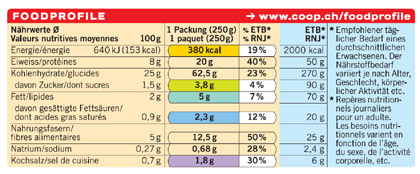 Grafische Formen und Symbole sind möglich. Zudem ist die Erwähnung von Referenzmengen in Bezug auf die Big 7 in der obligatorischen Nährwerttabelle oder die Angaben auf der Vorderseite im Rahmen der Wiederholung möglich. Der Wortlaut Referenzmenge für einen durchschnittlichen Erwachsenen (8400 kJ/2000 kcal) ist dabei zu verwenden (siehe Art. 32 Abs. 5 LMIV). Zudem ist die Angabe pro Portion oder Verzehrseinheit möglich (Art. 33 LMIV). Ausnahmen von der obligatorischen Nährwertwertdeklaration sind in Anhang V LMIV aufgeführt. Die obligatorische Nährwertdeklaration ist ab 13. Dezember 2016 verpflichtend (Art. 55 LMIV), sie kann aber ab sofort verwendet werden (Art. 54 Abs. 3 LMIV). Eine bereits vorhandene Nährwertdeklaration muss ab dem 13. Dezember 2014 dem neuen Recht entsprechen. Mindestschriftgrösse Die Pflichtangaben müssen auf der Verpackung oder dem daran befestigten Etikett mit einer Schriftgrösse von mindestens 1.2 mm, gemessen am kleinen x, angebracht werden (Art. 13 Abs. 2 LMIV). Bei Verpackungen, deren grösste Oberfläche weniger als 80 cm2 beträgt, kann die Mindestschriftgrösse 0.9 mm betragen. Wie an der Tagung ausgeführt wurde, ist jedoch der Begriff grösste Oberfläche auslegungsbedürftig; hierzu ist bereits ein liberal abgefasstes Interpretationspapier von FDE (FoodDrinkEurope, europäischer Verband der Lebensmittel- und Getränkeindustrie) erschienen. Allergenkennzeichnung Stoffe, die gemäss Anhang II LMIV Allergien oder Unverträglichkeiten auslösen, sind in der Zutatenliste künftig hervorzuheben (durch Schriftart, den Schriftstil oder die Hintergrundfarbe, siehe Art. 21 Abs. 1b LMIV) beispielsweise: Gewürze (enthalten Sellerie). Ist das gleiche Allergen in mehreren Zutaten oder Verarbeitungshilfsstoffen enthalten, muss die Kennzeichnung dies für jede dieser Zutaten / Verarbeitungshilfsstoffe deutlich machen. Auch bei offen angebotenen Produkten (z.B. in Bäckereien) wird die schriftliche Anbringung der Allergenkennzeichnung verpflichtend (Art. 44 Abs. 1a LMIV). Kennzeichnung von Lebensmittelimitaten Die Verwendung von sogenannten Lebensmittelimitaten muss nach dem neuen EUKennzeichnungsrecht in unmittelbarer Nähe zum Produktnamen (nicht zur Bezeichnung des Lebensmittels!) angegeben werden. Die Schriftgrösse der Imitatkennzeichnung muss mindestens 75% der Grösse des Produktnamens entsprechen (Anhang VI A 4a und b LMIV). Bei der Verwendung von sogenanntem Klebefleisch muss der Hinweis stehen aus Fleischstücken zusammengefügt oder aus Fischstücken zusammengefügt (beispielsweise bei Surimi-Garnelen). Herkunftsbezeichnung Die Herkunftsbezeichnung wird gemäss Art. 26 Abs. 2 LMIV künftig auch für Schweine-, Schaf-, Ziegen- und Geflügelfleisch verpflichtend (bei Rindfleisch besteht sie wegen der BSE-Krise aufgrund der Verordnung Nr. 1760/20003 bereits seit dem Jahr 2000). Zudem soll für andere Fleischarten, Fleisch als Zutat sowie Milch, Milch als Zutat, unverarbeitete Lebensmittel, Erzeugnisse aus einer Zutat sowie Zutaten, die über 50% des Lebensmittels ausmachen, binnen drei Jahren ein Bericht der Kommission erscheinen und dann über weitere Regelungen entschieden werden. Raffinierte pflanzliche Öle und Fette sind künftig mit der Angabe der speziellen pflanzlichen Herkunft zu versehen (Anhang VII A LMIV). Auslöser dieser neuen Regelung waren die Diskussionen um die Herkunft von Palmöl (Tropenwald-Rodungen für Palmöl-Plantagen).  Weitere wichtige Punkte des neuen Kennzeichnungsrechts betreffen das Einfrierdatum auf tiefgefrorenem Fleisch, Fleischprodukten und unverarbeiteten Fleischerzeugnissen oder die Angabe eines Warnhinweises bei koffeinhaltigen Lebensmitteln für Kinder, Schwangere und Stillende. Auf diese Neuerungen wurde in der Tagung jedoch nicht spezifisch eingegangen. Zusatzstoffe und Aromen Des Weiteren wurde der Rechtsrahmen für Zusatzstoffe und Aromen in der EU behandelt. Die Verordnung Nr. 1333/20084, die das EU-Zusatzstoffrecht neu geregelt und harmonisiert hat, gilt seit dem 20. Januar 2010. Aufgrund des Verbotsprinzips mit Erlaubnisvorbehalt mussten Positivlisten für die Anhänge II und III der Verordnung Nr. 1333/2008 erstellt werden. Diese Anhänge blieben bis im November 2011 leer, bis die Verordnungen Nr. 1129/20115 sowie Nr. 1130/20116 publiziert wurden, welche diese Anhänge definieren. Diese Veröffentlichungen bildeten den Grund für die Thematisierung des Zusatzstoffrechts an der Tagung. Die genannten Gemeinschaftslisten in den Anhängen II und III wurden auf Basis einer wissenschaftlichen Beurteilung der Europäischen Behörde für Lebensmittelsicherheit (EFSA) erstellt. Zugelassene Zusatzstoffe, Aromen und Enzyme dürfen nur eingesetzt werden, wenn sie technologisch notwendig, sicher und nicht irreführend sind. Anhang II (veröffentlicht als Verordnung Nr. 1129/2011) definiert die Liste der Lebensmittelzusatzstoffe in der EU und ihre Verwendungsbedingungen pro Lebensmittelkategorie. Er gilt ab 1. Juni 2013 (mit Ausnahmen) und ist wie folgt aufgebaut: Teil A: Einleitung; allgemeine Bestimmungen; zwei Listen von Lebensmitteln, in denen nach dem Migrationsgrundsatz (Carry Over) Zusatzstoffe oder Farbstoffe nicht zugelassen werden dürfen Teil B: Liste aller Zusatzstoffe Teil C: Festlegung von Zusatzstoffgruppen Teil D: Lebensmittelkategorien Teil E: Zugelassene Lebensmittelzusatzstoffe und Verwendungsbedingungen nach Lebensmittelkategorie Die Lebensmittelkategorien wurden neu erstellt, was in der Praxis zu Schwierigkeiten bei der Einordnung führen kann. Es wurden daher Leitlinien der Kommission in Aussicht gestellt, die für die Einordnung behilflich sein könnten. Anhang III der Verordnung Nr. 1333/2008 (publiziert als Verordnung Nr. 1130/2011) definiert eine Liste von Zusatzstoffen zur Verwendung in anderen Lebensmittelzusatzstoffen, Lebensmittelenzymen, Lebensmittelaromen und Nährstoffen. Er enthält verschiedene Übergangsvorschriften.  Weil in der Schweiz die Aromen ebenfalls zur Stoffklasse der Zusatzstoffe zählen (siehe Art. 2 Abs. 1 lit. l LGV7), wurde auch die EU-Aromenregelung behandelt, um den Vergleich mit der Schweiz herstellen zu können. In der EU werden die Aromen in der Verordnung Nr. 1334/20088 geregelt. Sie regelt die Verwendung von Aromen, Lebensmittelzutaten mit Aromaeigenschaften, Aromaausgangsstoffen sowie von Lebensmitteln, die Aromen oder Zutaten mit Aromaeigenschaften enthalten. Stoffe mit ausschliesslich salzigem, süssem oder saurem Geschmack, rohe Lebensmittel, nicht zusammengesetzte Lebensmittel oder Mischungen von u.a. frischen, getrockneten oder tiefgekühlten Gewürzen/Kräutern oder Teemischungen als solche (sofern sie nicht als Lebensmittelzutat verwendet werden) sind ausgenommen (Art. 2 VO Nr. 1334/2008). Auch bei den Aromen soll gemäss dieser Verordnung eine Positivliste entstehen, welche aufgrund von Sicherheitsbewertungen der EFSA erstellt wird. Dies gilt für folgende Stoffe: Aromastoffe, Aromaextrakte aus Nicht-Lebensmitteln, thermische Reaktionsaromen aus Nichtlebensmitteln und/oder nicht gemäss den Bedingungen nach Anhang V, Aromavorstufen aus Nichtlebensmitteln, sonstige Aromen sowie Ausgangsstoffe, die keine Lebensmittel sind (siehe Art. 9 VO 1334/2008). Die Veröffentlichung dieser Positivliste wird im Sommer 2012 erwartet und gilt 6 Monate nach Inkrafttreten. Die Aromen-Verordnung Nr. 1334/2008 unterscheidet für die Kennzeichnung lediglich zwischen Aromen und natürlichen Aromen. Die Angabe natürlich darf nur verwendet werden, wenn der Aromabestandteil ausschliesslich Aromaextrakte oder natürliche Aromastoffe enthält. Als natürliche Aromastoffe gelten Aromastoffe, die natürlich vorkommen und in der Natur nachgewiesen wurden (Art. 3 Abs. 2 lit. c VO 1334/2008). Wird auf eine namensgebende Quelle hingewiesen (z.B. natürliches Himbeeraroma), muss der Aromabestandteil zu mindestens 95% aus dieser Quelle (Himbeere) stammen. Die verbleibenden 5% müssen ebenfalls natürlichen Ursprungs sein. Werden weniger als 95% des Aromabestandteils aus einem Ausgangsstoff gewonnen und ist die Geschmacksnote leicht erkennbar, kann das Aroma als natürliches XY-Aroma mit anderen natürlichen Aromen deklariert werden. Stammt jedoch der Aromabestandteil aus verschiedenen Ausgangsstoffen und kann die Nennung dieser Ausgangsstoffe die Geschmacksnote nicht zutreffend beschreiben, darf nur die Angabe natürliches Aroma verwendet werden. An der Tagung wurde folgendes Beispiel dazu genannt: Der Aromabestandteil besteht zu 0% Gewichtsprozent aus Banane und zu 100% Gewichtsprozent aus anderen Ausgangsstoffen als Banane. Die Geschmacksnote ist Banane. Hier kann die Kennzeichnung nur lauten natürliches Aroma, Bananenaroma oder schlicht Aroma; natürliches Bananenaroma wäre unzulässig. Health Claims gesundheitsbezogene Angaben Der dritte Themenbereich, der an der Tagung behandelt wurde, betraf die gesundheitsbezogenen Angaben (health claims). Die Werbung für Lebensmittel mit funktionellen Angaben wird durch die Verordnung Nr. 1924/20069 (sogenannte health claim-Verordnung, HCVO) stark reglementiert und soll durch die Verabschiedung der sogenannten Art. 13- Liste (Positivliste zu allgemeinen gesundheitsbezogenen Angaben) nun eine wichtige, lange erwartete Vollendung erfahren. Diese Liste hätte bereits, gemäss Art. 13 Abs. 3 HCVO, bis 31. Januar 2010 verabschiedet werden sollen. Allerdings übertraf die Anzahl der Anträge der Mitgliedsländer - über 40000, die dann auf ca. 4000 konsolidiert wurden - alle Erwartungen, sodass die wissenschaftlichen Beurteilungen der EFSA wesentlich mehr Zeit in Anspruch genommen haben. Wie erwähnt, soll diese Liste nun in Kürze publiziert werden; sie wurde am 21. März 2012 vom zuständigen Ausschuss des Europaparlamentes gebilligt und enthält 222 erlaubte Werbeaussagen. Sobald die Liste veröffentlicht ist, haben die Lebensmittelunternehmen noch ein halbes Jahr Zeit, um bereits verpackte Produkte, die unerlaubte Aussagen tragen, zu verkaufen. Danach dürfen die nicht mehr zugelassenen Health Claims nicht mehr verwendet werden.  Trotz der Publikation dieser Art. 13-Liste bestehen noch wesentliche Baustellen in Bezug auf die vorgesehene Anwendung der Verordnung Nr. 1924/2006. Die Gemeinschaftsliste ist eigentlich noch nicht vollständig, weil die Claims zu den Botanicals (pflanzliche Stoffe) darauf fehlen. Die gesundheitsbezogenen Angaben zu den Botanicals werden von der EFSA gemäss einer Pressemitteilung der Kommission vom 27. September 2010 gesondert beurteilt und sollen später publiziert werden. Auch noch offen sind die Definitionen für die sogenannten Nährwertprofile. Gemäss Art. 4 HCVO sollen Lebensmittel, die nährwertund gesundheitsbezogene Angaben tragen, bestimmten Nährtwertprofilen genügen. Es sollen also Einschränkungen für Produkte, die nährwert- und gesundheitsbezogene Angaben tragen, festgelegt werden, da diese Produkte von den Konsumentinnen und Konsumenten als besonders wertvoll wahrgenommen werden könnten (Erwägungsgrund 10 der HCVO). Diese Nährwertprofile hätten bis 19. Januar 2009 festgelegt werden sollen, bestehen jedoch noch nicht. Deshalb ist es möglich, dass bei gewissen Produkten, die jetzt auf Basis der allgemeinen Art. 13-Liste gesundheitsbezogene Angaben tragen werden, diese Claims aufgrund der später veröffentlichten Nährwertprofile wieder entfernt werden müssen. In einem Referat der Firma Unilever wurden die Erfahrungen einer Firma beim Zulassungsverfahren sowie bei der Verwendung von zugelassenen Claims erläutert. Diese Erfahrungen sind, vorallem für kleinere Firmen, wenig ermutigend: sehr viele Anträge wurden von der EFSA negativ beurteilt; die Anforderungen an die wissenschaftliche Absicherung der Claims übersteigen wahrscheinlich die Möglichkeiten vieler KMUs. Allerdings können diese Unternehmen nach Verabschiedung der erwähnten allgemeinen Art. 13- Liste die entsprechenden Claims verwenden. Sich mit individuellen Claims nach Art. 13(5) oder Art. 14 HCVO auf dem Markt zu positionieren, dürfte jedoch angesichts der hohen Anforderungen an die wissenschaftliche Absicherung für KMUs sehr schwierig sein, was zu einer Wettbewerbsverzerrung führen kann. Wichtig ist in jedem Fall die Beachtung der mit dem Claim verbundenen Verwendungsbedingungen (inkl. genauem Wortlaut), wie der Referent von Unilever ausführte. Der von der Kommission definierte Wortlaut ist allerdings aus Sicht der Firma oftmals schwerfällig und nicht konsumentenfreundlich formuliert; trotzdem darf der Wortlaut des Claims nicht angepasst werden, auch wenn die Aussage dadurch nicht verändert würde. Politische Rahmenbedingungen Das letzte Referat des Tages stellte den Bezug zur Schweiz her, in dem der Referent vom BAG darlegte, wie sich die politischen Rahmenbedingungen und Entwicklungen auf das Schweizer Lebensmittelrecht auswirken oder noch auswirken werden. Unterstrichen wurde der Sinneswandel von Bundesrat und Parlament in den letzten Monaten, der dazu geführt hat, dass liberale Lebensmittelrechts-Konzepte, wie die unilaterale Einführung des Cassis-de-Dijon-Prinzips durch die Schweiz oder das angestrebte Freihandelssowie Gesundheitsabkommen mit der EU, politisch nun höchst umstritten sind, wie dies verschiedene Initiativen oder Motionen darlegen. Dass es zur Zeit gilt, sich bezüglich der Übernahme von EU-Recht auf das Nötigste zu beschränken, zeigen u.a. auch die Diskussionen in der vorberatenden Kommission des Nationalrates (Kommission für soziale Sicherheit und Gesundheit, SGK-N) zum Entwurf für ein neues Bundesgesetz über Lebensmittel und Gebrauchsgegenstände (E-LMG10): So gab es einen Antrag, die Vorlage vollständig zu überarbeiten und nur das unumgängliche EU-Recht zu übernehmen (siehe Medienmitteilung vom 3. Februar 2012 auf Curia Vista, Geschäft 11.034). Dieser Antrag wurde nur durch Stichentscheid des Präsidenten der Kommission abgelehnt. Bei der Revision und Weiterentwicklung des Schweizer Lebensmittelrechts geht es laut Ausführungen des BAG darum, einerseits keine Handelshemmnisse mit der EU entstehen zu lassen, andererseits kein unnötiger Zusatzaufwand für KMUs aufzubauen und die Stimmungen in der Politik zu berücksichtigen. In Bezug auf die während der Tagung dargelegten Themen Kennzeichnung, Zusatzstoffe und Health Claims werden deshalb diejenigen EU-Bestimmungen übernommen, deren Nicht-Übernahme zu Handelshemmnissen führen könnte. So soll beispielsweise die Nährwertkennzeichnung oder die Schriftgrösse wie im neuen EURecht übernommen werden. Auch ist eine Totalrevision der Schweizerischen Zusatzstoffverordnung ZuV11 in Planung, um die EU-Listen in das Schweizerische Recht zu überführen (inkl. Lebensmittelkategorien, die nicht identisch mit den aktuellen Kategorien in der ZuV sind); die Anhörung dazu ist in der zweiten Hälfte 2012 geplant. Abschliessend ist ein Ausblick über den Fahrplan zur Totalrevision des LMG gemacht worden: die Schlussabstimmung wird, gemäss heutigem Stand, etwa Mitte 2013 erfolgen, die Vernehmlassung zum Verordnungsrecht soll dann in der zweiten Hälfte des Jahres 2013 und das Inkrafttreten des revidierten LMG und des darauf abgestützten Verordnungsrechts Ende 2014 oder anfangs 2015 erfolgen. Wenn sich die politische Stimmung allerdings wieder ändert und die Abkommen mit der EU doch abgeschlossen werden, würde dies grundlegende Auswirkungen auf diese Prozesse haben. Auch für 2013 ist wieder eine Tagung geplant, die aktuelle lebensmittelrechtliche Themen und Fragestellungen aufgreifen wird. Fussnoten: 1 Verordnung (EG) Nr. 178/2002 des Europäischen Parlaments und des Rates vom 28. Januar 2002 zur Festlegung der allgemeinen Grundsätze und Anforderungen des Lebensmittelrechts, zur Errichtung der Europäischen Behörde für Lebensmittelsicherheit und zur Festlegung von Verfahren zur Lebensmittelsicherheit, ABl. L 31 vom 1.2.2002, S. 1. 2 Verordnung (EU) Nr. 1169/2011 des Europäischen Parlaments und des Rates vom 25. Oktober 2011 betreffend die Information der Verbraucher über Lebensmittel und zur Änderung der Verordnungen (EG) Nr. 1924/2006 und (EG) Nr. 1925/2006 des Europäischen Parlaments und des Rates und zur Aufhebung der Richtlinie 87/250/EWG der Kommission, der Richtlinie 90/496/EWG des Rates, der Richtlinie 1999/10/EG der Kommission, der Richtlinie 2000/13/EG des Europäischen Parlaments und des Rates, der Richtlinien 2002/67/EG und 2008/5/EG der Kommission und der Verordnung (EG) Nr. 608/2004 der Kommission, ABl. L 304 vom 22.11.2011, S. 18. 3 Verordnung (EG) Nr. 1760/2000 des Europäischen Parlaments und des Rates vom 17. Juli 2000 zur Einführung eines Systems zur Kennzeichnung und Registrierung von Rindern und über die Etikettierung von Rindfleisch und Rindfleischerzeugnissen, ABl. L 204 vom 11.8.2000, S.1. 4 Verordnung (EG) Nr. 1333/2008 des Europäischen Parlaments und des Rates vom 16. Dezember 2008 über Lebensmittelzusatzstoffe, ABl. L 354 vom 31.12.2008, S. 16. 5 Verordnung (EU) Nr. 1129/2011 der Kommission vom 11. November 2011 zur Änderung des Anhangs II der Verordnung (EG) Nr. 1333/2008 des Europäischen Parlaments und des Rates im Hinblick auf eine Liste der Lebensmittelzusatzstoffe der Europäischen Union, ABl. L 295 vom 12.11.2011, S. 1. 6 Verordnung (EU) Nr. 1130/2011 der Kommission vom 11. November 2011 zur Änderung des Anhangs III der Verordnung (EG) Nr. 1333/2008 des Europäischen Parlaments und des Rates über Lebensmittelzusatzstoffe im Hinblick auf eine Liste der Europäischen Union der für die Verwendung in Lebensmittelzusatzstoffen, Lebensmittelenzymen, Lebensmittelaromen und Nährstoffen zugelassenen Lebensmittelzusatzstoffe, ABl. L 295 vom 12.11.2011, S. 178. 7 Lebensmittel- und Gebrauchsgegenständeverordnung vom 23. November 2005 (LGV), SR 817.02. 8 Verordnung (EG) Nr. 1334/2008 des Europäischen Parlaments und des Rates vom 16. Dezember 2008 über Aromen und bestimmte Lebensmittelzutaten mit Aromaeigenschaften zur Verwendung in und auf Lebensmitteln sowie zur Änderung der Verordnung (EWG) Nr. 1601/91 des Rates, der Verordnungen (EG) Nr. 2232/96 und (EG) Nr. 110/2008 und der Richtlinie 2000/13/EG, ABl. L 354 vom 31.12.2008, S. 34. 9 Verordnung (EG) Nr. 1924/2006 des Europäischen Parlaments und des Rates vom 20. Dezember 2006 über nährwert- und gesundheitsbezogene Angaben über Lebensmittel, ABl. L 404 vom 30.12.2006, S. 9. 10 Entwurf für ein Bundesgesetz über Lebensmittel und Gebrauchsgegenstände (E-LMG), BBl 2011 5661. 11 Verordnung des EDI vom 22. Juni 2007 über die in Lebensmitteln zulässigen Zusatzstoffe (Zusatzstoffverordnung, ZuV), SR 817.022.31. (Text: ZHAW) | ||||
